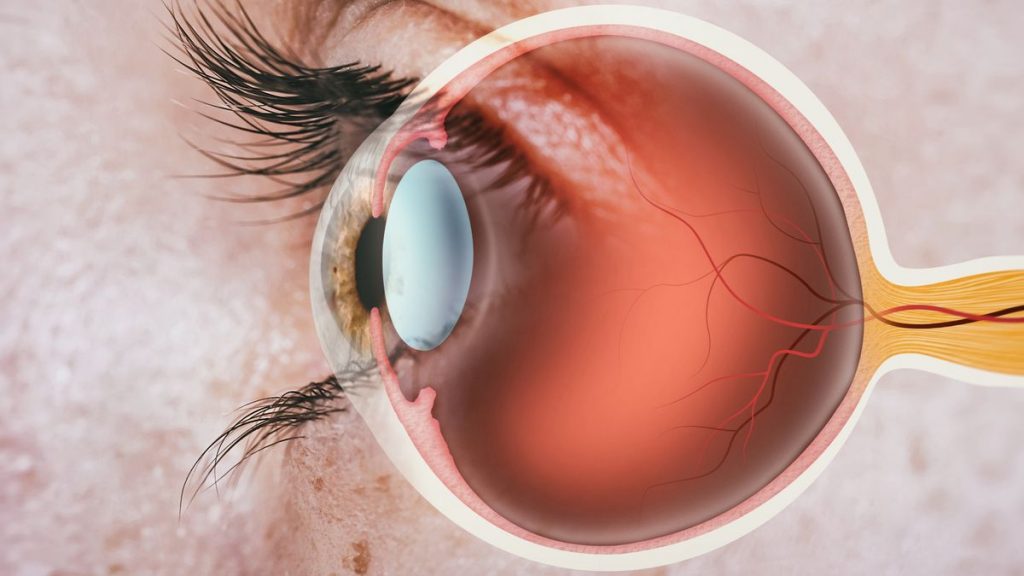
Dans le cadre d’expériences qui pourraient bouleverser la recherche sur le cerveau et la vision, des scientifiques ont ramené à la vie des cellules neuronales sensibles à la lumière dans les yeux d’un donneur mort quelques heures auparavant.
« Nous avons pu réveiller les cellules photoréceptrices de la macula humaine »
Certains organes humains restent fonctionnels et viables pour une transplantation plusieurs heures après la mort du donneur. Malheureusement, cela ne s’applique généralement pas aux tissus du système nerveux, qui sont parmi les premiers à s’éteindre complètement en raison du manque d’oxygène.
Pour cette nouvelle étude publiée dans la revue Nature, Fatima Abbas et ses collègues de l’université de l’Utah ont utilisé la rétine comme modèle du système nerveux central humain (qui renferme des milliards de neurones transmettant les informations sensorielles sous forme de signaux électriques) afin d’étudier la mort neuronale et d’identifier des moyens potentiels de restaurer ce type de cellules.
Ces travaux ont conduit au développement d’une nouvelle approche, qui permettra aux scientifiques d’étudier la vision humaine dans des yeux prélevés post-mortem.
« Nous avons pu réveiller les cellules photoréceptrices de la macula humaine, qui est la partie de la rétine responsable de notre vision centrale et de notre capacité à voir les détails fins et les couleurs », explique Abbas. « Dans les yeux obtenus jusqu’à cinq heures après le décès d’un donneur d’organes, ces cellules ont réagi à la lumière vive, aux lumières colorées et même à des flashs lumineux très faibles. »

Une prouesse technique
Si l’équipe est rapidement parvenue à ranimer ces cellules photoréceptrices en rétablissant un pH et un niveau d’oxygénation normaux, ces dernières n’étaient toutefois plus capables de communiquer avec les autres cellules de la rétine. Afin de surmonter ce problème, ils ont utilisé des yeux prélevés moins de 20 minutes à compter du décès, qui ont été placés dans une unité de transport spéciale permettant de les réoxygéner et de leur apporter différents nutriments. Un dispositif stimulant la rétine et mesurant l’activité électrique de ses cellules a ensuite été utilisé.
Grâce à cette approche, un signal électrique spécifique observé dans les yeux vivants, connu sous le nom « d’onde b », a pu être restauré. Selon les chercheurs, il s’agit du premier enregistrement de cette dernière réalisé à partir de la rétine centrale d’yeux humains post-mortem.
« Nous avons réussi à faire communiquer de nouveau les cellules des différentes couches de la rétine centrale entre elles, comme elles le font dans l’œil vivant afin d’assurer la vision humaine », détaille Frans Vinberg, co-auteur de l’étude. « Des travaux antérieurs avaient permis de restaurer une activité électrique très limitée dans les yeux de donneurs d’organes, mais cela n’avait jamais été réalisé dans la macula, et jamais à cette échelle. »
Des implications majeures
Promettant un allongement substantiel de la durée de vie des organes transplantables, une telle approche pourrait notamment faciliter l’étude d’autres tissus neuronaux du système nerveux central et aider les scientifiques à mieux comprendre les maladies neurodégénératives. Y compris les maladies rétiniennes à l’origine d’une perte partielle ou totale de la vision, telles que la dégénérescence maculaire liée à l’âge.
« À l’avenir, nous pourrons utiliser cette approche pour développer des traitements visant à améliorer la vision et la signalisation lumineuse dans les yeux atteints de maladies maculaires », explique Anne Hanneken, du Scripps Research Institute.
Le nouveau protocole promet également de réduire la dépendance à l’égard des modèles animaux, qui ne fournissent pas toujours des résultats applicables à l’Homme. Désormais, les chercheurs pourront tester de nouvelles thérapies potentielles sur des cellules oculaires humaines fonctionnelles, ce qui accélérera le développement des médicaments.
Par Yann Contegat, le
Source: Cosmos Magazine
Étiquettes: vie, neurones, oeil, rétine
Catégories: Actualités, Sciences
