Des chercheurs du MIT ont démontré qu’une enzyme appelée HDAC1 aidait à réparer les dommages causés à l’ADN neuronal et à lutter contre le déclin cognitif lié à l’âge. Une découverte représentant un véritable espoir pour les patients atteints de maladies neurodégénératives, comme Alzheimer.
Une étude charnière
Si les lésions de l’ADN sont communes à l’ensemble de nos cellules, notre organisme peut, jusqu’à un certain âge, les réparer assez efficacement. Malheureusement, cette capacité s’affaiblit avec le temps, entraînant de nombreux symptômes du vieillissement que nous ne connaissons que trop bien. Dans le cadre de cette nouvelle étude publiée dans la revue Nature Communications, une équipe de chercheurs du MIT a découvert que la réactivation d’une certaine enzyme améliorait la réparation des dommages causés à l’ADN neuronal, et permettait de ce fait de lutter contre le déclin cognitif lié à l’âge.
Alors que de précédents travaux avaient montré que cette enzyme, appelée HDAC1 semblait être impliquée dans la réparation de l’ADN neuronal, dans le cadre de cette nouvelle étude, l’équipe a examiné ce qui se passait lorsque l’HDAC1 ne faisait pas son travail.
Pour ce faire, l’équipe a comparé l’évolution de souris génétiquement modifiées déficientes en HDAC1 à celle de souris saines. S’il n’existait aucune différence en termes de dommages causés à l’ADN ou de comportement entre les deux groupes durant la phase de croissance des animaux, le déclin est ensuite devenu évident.
Les chercheurs ont découvert que les souris plus âgées déficientes en HDAC1 présentaient des quantités plus importantes de dommages à l’ADN neuronal ainsi qu’une plasticité synaptique, caractérisant le fait que le cerveau modifie les connexions entre les neurones pour apprendre et se souvenir, réduite, ce qui se traduisait par de moins bonnes performances dans les tests de mémoire et de navigation spatiale.
Des fonctions cognitives largement améliorées chez les spécimens âgés grâce à la réactivation de l’HDAC1
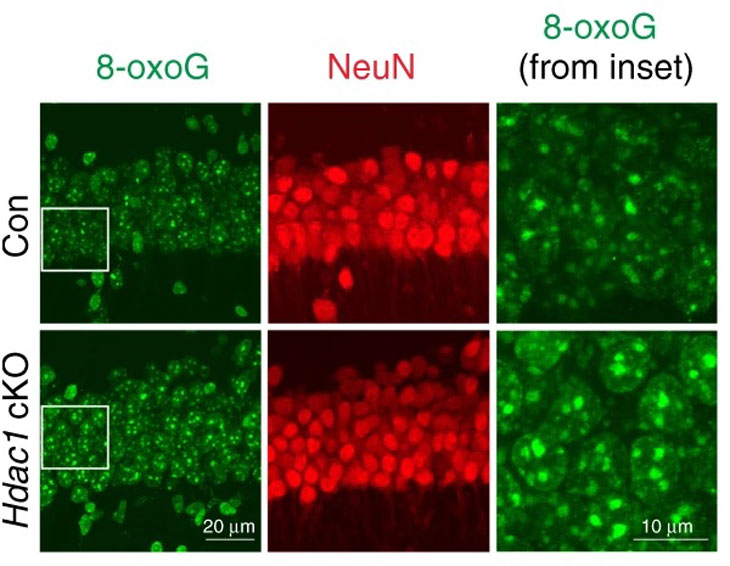
En examinant les rongeurs de plus près, l’équipe a découvert qu’ils présentaient des lésions de 8-oxo-guanine, un type spécifique de dommage à l’ADN causé par l’oxydation. Sachant que des niveaux élevés de ce type de lésions ont également été observés chez des patients atteints de la maladie d’Alzheimer.
« Il semble que l’HDAC1 soit vraiment une molécule anti-âge », estime Li-Huei Tsai, auteur principal de l’étude. « Je pense qu’il s’agit d’une découverte de biologie fondamentale disposant de très larges applications, étant donné qu’une grande partie des maladies neurodégénératives humaines ne surviennent que pendant le vieillissement. L’activation de l’HDAC1 se révèlerait sans doute bénéfique dans de nombreux cas. »
Pour aller plus loin, les chercheurs ont ensuite essayé de traiter la maladie en utilisant de l’exifone, composé médicamenteux activant l’HDAC1 et utilisé par le passé pour traiter la démence. Celui-ci a été administré à des souris atteintes d’Alzheimer et des souris âgées en bonne santé, et l’équipe a constaté que, dans l’ensemble, il réduisait les lésions de l’ADN dans le cerveau, améliorant ainsi les fonctions cognitives comme la mémoire.
Toutefois, aussi prometteur que l’exifone puisse paraître, ce type de traitement est loin d’être idéal (celui ayant en effet provoqué des lésions hépatiques chez certains patients). Néanmoins, les chercheurs affirment que la confirmation du rôle de l’HDAC1 dans le renversement du déclin cognitif signifie que d’autres médicaments remplissant la même fonction pourraient être développés.
« Cette étude positionne réellement l’HDAC1 comme une nouvelle cible potentielle de médicaments pour les phénotypes liés à l’âge, ainsi que pour les pathologies et phénotypes associés à la neurodégénérescence », conclut Tsai.

Par Yann Contegat, le
Source: New Atlas
Étiquettes: adn, enzyme, alzheimer, neurone, neurodégénérescence, maladie neurodégénératives, déclin cognitif, cerveau
Catégories: Actualités, Santé
