
Des expériences ont montré que lorsqu’elles étaient confinées, les molécules d’eau pouvaient se comporter à la fois comme un solide et un liquide. Un état étrange connu sous le nom de « pré-fusion ».
À mi-chemin
Les différences apparentes entre glace et eau liquide trouvent leur origine à l’échelle microscopique. Dans le premier cas, les molécules s’organisent en structures rigides et ordonnées, tandis que dans le second, elles flottent librement, avec des liaisons hydrogène se formant et se rompant constamment. L’état récemment décrit se situe grosso modo à mi-chemin.
« La pré-fusion implique la fusion de H2O incomplètement lié par des ponts hydrogène avant que la glace ne commence à fondre », explique Makoto Tadokoro, chimiste à l’université des sciences de Tokyo. « Il s’agit essentiellement d’une nouvelle phase de l’eau où coexistent des couches de H2O gelées et se déplaçant lentement. »
Les expériences réalisées ont impliqué de « l’eau lourde », dans laquelle les atomes d’hydrogène sont remplacés par du deutérium, isotope de l’hydrogène au coeur des réactions de fusion nucléaire, dont le noyau contient un seul neutron. Ce « D2O » a été injecté dans les minuscules canaux (1,6 nanomètre de large) de cristaux en forme de bâtonnets, qui ont été congelés puis lentement réchauffés.
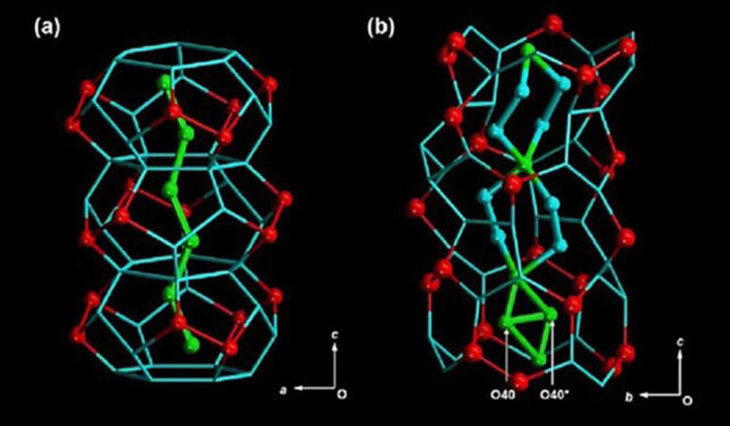
L’utilisation d’une technique d’imagerie avancée, connue sous le nom de « spectroscopie par résonance magnétique nucléaire », a révélé que les molécules d’eau lourde formaient alors une structure à trois couches, avec différents types de mouvements et d’interactions dans chacune d’elles.
Exploiter les comportements exotiques de l’eau
Lorsqu’elle est confinée à l’échelle nanométrique, l’eau peut se comporter de manière assez déroutante. Si ses propriétés électriques peuvent changer, elle peut également devenir « impossible à congeler » à des températures proches du zéro absolu (−273,15 °C), ou à l’inverse se solidifier alors qu’elle devrait normalement entrer en ébullition.
Selon les auteurs de la nouvelle étude, publiée dans le Journal of the American Chemical Society, l’exploitation de ces comportements exotiques pourrait notamment permettre d’améliorer le stockage de l’hydrogène ou du méthane.
En début d’année, des scientifiques avaient créé une nouvelle glace « extraterrestre » en laboratoire.
