Organe le plus important du corps humain, le coeur est aussi extrêmement fragile. Tant et si bien que la demande de greffes cardiaques demeure une préoccupation majeure des services de santé. Mais désormais, grâce à une équipe de chercheurs, il devrait bientôt être possible de littéralement faire pousser ces organes. SooCurious vous en dit plus sur leurs travaux.
Dans le monde, 25 millions de personnes souffrent d’insuffisance cardiaque, sans toutefois pouvoir toujours compter sur une greffe salvatrice. Ainsi, à titre d’exemple, le nombre de personnes en attente d’une greffe en France en 2014, était de 361 et plus de 20 % de ces patients sont morts faute d’avoir pu obtenir un nouveau coeur. Ce constat, aussi alarmant soit-il, pourrait toutefois changer à l’avenir. Car une équipe de chercheurs américains tient peut-être une solution incroyable.
 Une femme souffre du coeur via Shutterstock
Une femme souffre du coeur via Shutterstock
Pour cette étude en laboratoire, des scientifiques du Massachusetts General Hospital et de l’école de médecine d’Harvard ont réussi l’exploit de pousser des coeurs humains à se régénérer eux-mêmes à partir des cellules de donneurs.
Lors de l’expérimentation, les chercheurs ont utilisé 73 coeurs humains non utilisables pour une transplantation. Après avoir été soigneusement immergés dans des solutions qui les ont débarrassés de toutes les cellules pouvant provoquer une réponse immunitaire négative, les organes n’étaient plus composés que de leur plus simple structure.
Un coeur « vidé »
Les scientifiques ont alors introduit dans les coeurs des cellules souches pluripotentes induites (CSPi), issues de cellules de peau humaine d’adultes, reprogrammées pour reproduire un tissu musculaire cardiaque fonctionnel.
Placées dans les organes humains et plongées dans une solution nutritive, les CSPi se sont alors développées en deux types de cellules cardiaques. Ainsi, après deux semaines, les réseaux cellulaires cultivés ont commencé à ressembler à ceux d’un coeur correctement structuré, même s’ils n’étaient pas entièrement formés. Finalement, une fois alimentés par une décharge électrique, les organes ont commencé à battre.
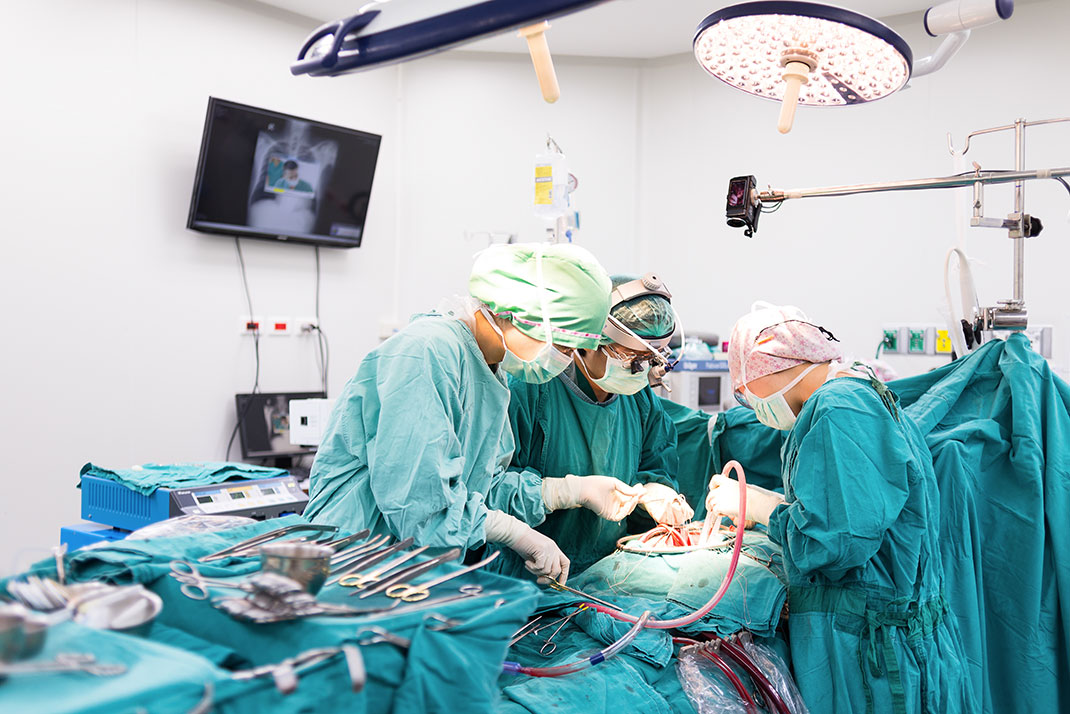 Une opération du coeur via Shutterstock
Une opération du coeur via Shutterstock
L’intérêt de cette réalisation est que les cellules cardiaques cultivées sont reconnues par le système immunitaire comme issues du même organisme, puisque provenant du même patient. Elles sont donc beaucoup moins susceptibles, comme le coeur implanté, d’être rejetées par le receveur de la greffe.
« Parmi les prochaines étapes que nous poursuivons, se trouve l’amélioration des méthodes consistant à générer plus de cellules cardiaques », explique Jacques Guyette, chercheur biomédical au centre MGH pour la médecine dégénérative et auteur principal de l’étude. Il ajoute d’ailleurs que même si l’étude a permis la fabrication de 500 millions de cellules cardiaques, faire pousser un coeur entier en nécessiterait « des dizaines de milliards ».
Jacques Guyette
Même si l’étude n’a pas permis de faire pousser entièrement un coeur humain fonctionnel, les travaux des chercheurs se sont approchés plus près de cet objectif que n’importe quelle autre expérience auparavant. A terme, il devrait donc être possible de « cultiver » entièrement des coeurs en laboratoire à partir des cellules souches de donneurs, avant de leur implanter leur nouvel organe.
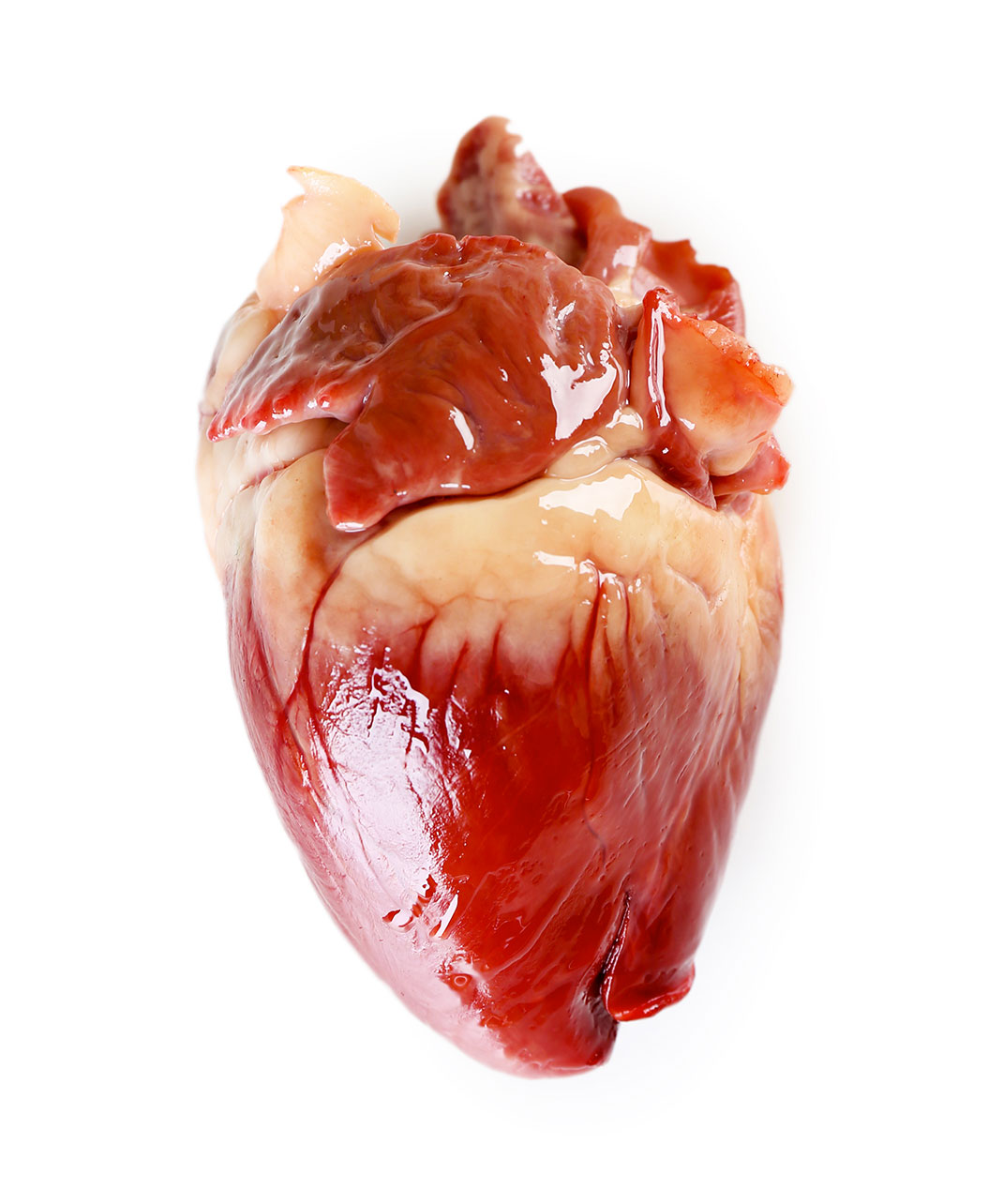 Un coeur humain via Shutterstock
Un coeur humain via Shutterstock
Ces travaux sont réellement très encourageants pour la médecine et pour la vie des personnes fragiles du coeur. Surtout, ils illustrent tous les progrès que permet la science lorsqu’il s’agit de sauver des vies humaines. Si les progrès médicaux vous intéressent, découvrez également cette technique d’impression 3D qui permet de créer des organes fonctionnels.
Par Maxime Magnier, le
Source: iflscience
Étiquettes: étude, science, médecine, cellules, coeur
Catégories: Sciences, Actualités


